| Titel: | Ueber die galvanoplastischen Operationen des geodätischen Bureaus der Vereinigten Staaten; von Georg Mathiot, Director des galvanoplastischen Laboratoriums. |
| Fundstelle: | Band 138, Jahrgang 1855, Nr. LXXXIX., S. 350 |
| Download: | XML |
LXXXIX.
Ueber die galvanoplastischen Operationen des
geodätischen Bureaus der Vereinigten Staaten; von Georg Mathiot, Director des galvanoplastischen
Laboratoriums.
Aus Silliman's american Journal of Science and Arts, Mai 1853, S. 305.
Mit Abbildungen auf Tab.
V.
Mathiot, über die galvanoplastischen Operationen des geodätischen
Bureaus der Vereinigten Staaten.
Mittel das Anhängen des Niederschlags an der Matrize zu
verhüten. – Die Elektrometallurgie fordert, daß das abgelagerte
Metall seine Cohäsion vollkommen beibehalte. Wenn ein solcher Niederschlag von
Kupfer auf einer reinen Platte desselben Metalles hervorgebracht wird, so muß
natürlich das abgelagerte Metall mit der ursprünglichen Platte zusammenhängen,
wodurch eine mit Mühe gravirte Platte in eine bloße Metallmasse umgewandelt würde.
So lange man also nicht im Besitze von Mitteln ist, diesem Anhaften zu begegnen,
kann von einer Elektrotypie (Galvanoplastik) nicht die Rede seyn. Die verschiedenen
Verfahrungsweisen gegen diesen Mißstand beruhen sämmtlich auf der Zwischenlagerung
einer dünnen Haut anderweitigen Materials, um der unmittelbaren Berührung von
Niederschlag und Matrize vorzubeugen.
Hr. Smee schlägt die Benützung der Lufthaut vor, welche
polirten Metallen fest anhaftet (was sich auffallend zeigt, wenn man eine polirte
Messerklinge naß zu machen versucht). Um diese Lufthaut zu erhalten, soll nach ihm
die zuerst vollkommen hergerichtete Platte, bevor man sie in das elektrotypische Bad
bringt, einige Tage in einem kühlen und feuchten Keller liegen.
Rauch, Graphit, Oele, Wachs etc. wurden ebenfalls als Ueberzug der Plattenfläche
vorgeschlagen.
Folgende, im brittischen topographischen Bureau befolgte Methode ist vielleicht die
beste unter allen diesen. Die Platte wird zuerst gut mit Oel eingerieben und dann
das Oel mit weichem Brod sorgfältig abgewischt. Nun erhitzt man sie etwas über den
Schmelzpunkt des Wachses und drückt einen Kuchen von weißem Wachs gegen den Rand. Da
das Oel die Luft von der Platte vertrieben hat, so überzieht das Wachs dieselbe
leicht in einer äußerst dünnen Schicht; jeder Ueberschuß desselben wird dann mit
feiner Leinwand (ohne Gefäsel) abgewischt. Bevor man die Platte in den Trog bringt,
muß man sie abkühlen lassen.
Es verstößt aber gegen die Grundsätze der auf atomweiser Ueberlagerung beruhenden
Elektrotypie, eine feingravirte Platte einzuschmieren. Bei dem Verfahren Smee's bleiben in den feinen Linien der Gravirung
Lufblasen zurück und verstümmeln folglich die Copie; überdieß wird die Oberfläche
der neuen Platte wellenförmig, in Folge der Bewegung der Luftschicht bei der ersten
Ablagerung von Kupfer. – Bei dem Wachsverfahren ist es fast unmöglich, jede
Linie von überschüssigem Wachs zu befreien. – Diese verschiedenen Methoden
sind also sehr unsicher. Man hat stets die Beobachtung gemacht, daß wenn das
abgelagerte Metall in seinen mechanischen Eigenschaften nicht
mangelhaft war, es sehr stark an dem Original haftete, und die Platten
heftig geschüttelt, erhitzt und geklopft werden mußten, um sie auseinander zu
bringen. War aber das abgelagerte Metall von sehr guter Qualität, dann war die
Trennung oft unmöglich.
Es war zu hoffen, daß sich eine Substanz ermitteln läßt, welche gleichförmig und
schwach auf die gravirte Platte wirkt, und, indem sie die homogene Anziehung der
Theilchen an der Oberfläche aufhebt, durch chemische Vereinigung mit denselben eine
unlösliche und zerreibliche Verbindung bildet, die der Platte nur schwach adhärirt.
Ich wählte zum Versuch das Jod, weil es in Wasser nur wenig löslich ist, ein hohes
Atomgewicht hat, und unschädlich ist. Eine Kupferplatte wurde wohl gereinigt dem
Joddampf ausgesetzt und elektrotypirt; die Ablagerung trennte sich leicht von ihr.
Dieß wurde mehrere Hundertmal mit gleichem Erfolge wiederholt.
Wenn große Platten für die Anwendung von Joddämpfen gereinigt wurden, zeigte es sich,
daß während der Reinigung des einen Theiles der andere anlief, daher keine
gleichmäßige Wirkung des Jods erzielt werden konnte. Dieses führte darauf, die
Platten zuerst zu versilbern und dann zu jodiren; eine versilberte Platte wurde
daher mit weingeistiger Lösung von Jod gewaschen und dann elektrotypirt; das
Elektrotyp löste sich von der Matrize noch leichter ab als vorher, indem das
Jodsilber die Adhärenz besser verhinderte als das Jodkupfer. Bald zeigte sich
jedoch, daß eine an einem trüben Tage präparirte Platte sich nicht so leicht
lostrennte, als wenn das Zurichten bei Hellem Himmel vorgenommen wurde, und Versuche
ergaben, daß eine zuerst jodirte und dann den Sonnenstrahlen ausgesetzte Platte sich
mit großer Leichtigkeit ablösen ließ; wogegen eine Platte welche an einem
regnerischen Tage jodirt und dann einige Stunden in ein dunkles Zimmer gestellt
wurde, bevor man sie in das (galvanoplastische) Bad brachte, so fest haftete, daß
man, um sie von der Matrize zu trennen, zu den alten Mitteln des Erhitzens und
Rüttelns seine Zuflucht nehmen mußte.
Seitdem wurde das Jodiren und Belichten an einer sehr großen Anzahl fein gravirter
Platten vollzogen, und niemals zeigte sich auch nur die geringste Schwierigkeit bei
der Trennung der Platten, wenn nur die gehörige Dicke der Copie erzielt worden
war.
Beim Präpariren unserer größten Platten von 10 Quadratfuß Oberfläche benutzte ich
eine Auflösung von 1 Gran Jod in 20000 Gran starkem Alkohol. Wenn ein Gran der
Lösung erforderlich ist, um einen Quadratfuß zu benetzen, so ist auf diesem nur
1/2000 Gran Jod. Da aber das Jod mit dem Alkohol rasch verdampft, so befindet sich
auf 1 Quadratfuß wahrscheinlich nicht mehr als 1/1000000 Gran Jod. Nimmt man das
Gewicht eines Kubikzolles Jod zu 1250 Gran an und setzt voraus, daß es auf der
Silberfläche in seinem ursprünglichen Zustande bleibt, anstatt Jodsilber zu bilden,
so ergibt sich 1,250 × 144 × 100,000 = 18,000,000,000, also bloß ein
achtzehntausendmilliontel Zoll für die Dicke der Jodschicht. Aber selbst angenommen,
daß die Sonnenstrahlen das Jodsilber zersetzen, und das Jod als Dampf auf der Platte
zurücklassen, so wird die Dicke der Jodschicht nur einen vierundvierzigmilliontel
Zoll betragen, also in mechanischer Hinsicht gar nicht in Betracht kommen.
Um den Einfluß dieser chemischen Zubereitung der Platte auf die Schärfe der gravirten
Linien zu ermitteln, wurde eine Gravirung siebenmal von Platte auf Platte
übergetragen, ohne daß die schärfste vergleichende Untersuchung der Abdrücke von der
letzten und der ersten Platte einen Unterschied herausstellte.
Zeit und Kosten der Elektrotypie. – Hr. Smee und Andere haben gezeigt, daß die Güte des
Elektrometalls (galvanisch gefällten Metalls) von gewissen Verhältnissen zwischen
der Schnelligkeit der Bildung der Platte und der Concentration der Lösung, worin sie
dargestellt wurde, abhängt. Da kleine Quantitäten von Elektricität leicht in
Bewegung gesetzt werden, so kann man kleine Elektrotype in 6–8 Tagen machen.
Um große Platten in kurzer Zeit zu erhalten, braucht man starke Ströme. Die
entsprechende größere effective elektrische Wirkung zu erhalten, zeigte sich aber
etwas schwierig. In dem Aide-mémorie der
brittischen Artillerie findet sich die Angabe, daß in der galvanoplastischen Anstalt
des topographischen Bureaus ein Pfund Kupfer sich in 24 Stunden auf einer Platte von
8 Quadratfuß niederschlug, und daß bloß durch fortgesetztes Umrühren der
elektrolytischen Lösung die Platten zähe genug wurden, um das Hämmern auszuhalten.
Auf diese Weise wären 45 Tage erforderlich, um eine 1/8 Zoll dicke Platte zu machen.
Meines Wissens ist vor
Anwendung des nun zu beschreibenden Verfahrens dieses Resultat weder in Bezug auf
die Zeit noch auf die Qualität des Metalls übertroffen worden.
Das erste Mittel, welches in Vorschlag gebracht wurde, um in derselben Zeit eine
größere Ablagerung zu erhalten, besteht in der Vergrößerung der Batterie; dadurch
kann aber der gewünschte Zweck nicht erreicht werden. Um dieses deutlich zu machen,
benutze ich die Formel von Ohm, welcher zeigte, daß der
Effect des Stromes irgend einer Batterie direct der elektromotorischen Kraft, und
umgekehrt dem ihr dargebotenen Widerstand proportional ist, was sich durch die
Gleichung E/(R + r) = Q ausdrücken läßt, in
welcher E die elektromotorische Kraft oder die
Verwandtschaft der Säure zum Zink, R + r den Widerstand
bedeutet; R ist der Widerstand in der zwischen den
positiven und negativen Elementen der Batterie befindlichen Flüssigkeit, r der Widerstand im Schließungsbogen, und Q die resultirende Arbeit, d.h. die Quantität des
erzielten Stromes. Der Widerstand ist erwiesenermaßen zur Länge der Leiter im
geraden, aber zum Querschnitt derselben im umgekehrten Verhältnisse.
E hängt von den chemischen Beziehungen der verwendeten
Metalle ab, ist also für dieselben constant; Q läßt sich
folglich nur auf die Art mit Vortheil ändern, daß man R
und r ändert. Da R den
Widerstand in der Batterie bezeichnet, so ist eine Vergrößerung der Platten mit
einer Vergrößerung des Querschnittes der Flüssigkeit gleichbedeutend, und der
Widerstand R wird dann kleiner. Der Ausdruck E/(R + r) = Q zeigt nun, daß wenn
der Widerstand in der Batterie im Verhältniß zum Widerstande außerhalb klein ist,
man von der Vergrößerung der Batterieplatten nur wenig Gewinn an Wirkung zu erwarten
hat.
Um den Werth von R in Beziehung auf r zu finden, wurde eine Batterie construirt, welche die
Sammlung und Messung der entwickelten Gase gestattete. Brachte man die Platten (der
Zerlegungszelle) in unmittelbare Berührung, und wurde die in 30 Minuten entwickelte
Gasmenge als Einheit der Wirkung genommen, so war in diesem Falle, da der Strom bloß
durch die Batterie zu gehen hatte, der durch r
angedeutete Widerstand = 0, also Q =E/R = 1. Nun wurde die
Batterie mit einem Paar Elektroden verbunden, die in einer Auflösung von
schwefelsaurem Kupfer, mit Schwefelsäure angesäuert, standen, welche saure Mischung
alle Schriftsteller über Elektrometallurgie behufs der Erzielung guten Metalles vorschreiben, Das nun
binnen 30 Minuten entwickelte Gas war bloß 1/20 der vorigen Menge; also hatte der
Widerstand von r die Größe von Q auf 1/20 herabgebracht, mithin war E/(R + r) = Q = E/20 R, also r = 19 R. Um nun den Effect zu erhalten, welcher mittelst
Vergrößerung der Batterie zu erzielen ist, haben wir Q
=1/(1/m + 19). Ist m = 1, so wird Q = 0,05; für
m = 4 ist Q = 0,0524
u.s.w., was zeigt, daß der Gewinn zu klein ist, um die Vergrößerung der Batterie zu
lohnen. Diese Berechnungen gelten für kleine Batterie-Platten; bei großen
müssen die gegenseitigen Entfernungen derselben vergrößert werden, und damit wächst
also der Widerstand, statt abzunehmen. Bloße Vergrößerung der Batterie ist folglich
nicht hinreichend, um die Zeit des Elektrotypirens abzukürzen.
Hr. Smee hat die negative Platte der Batterie mit
pulverförmigem Platin überzogen und so eine sehr starke Wirkung erzielt. Ist die
Platte frisch platinirt, so wirkt sie heftig und entwickelt Ströme von Wasserstoff;
aber in Folge der Verunreinigungen des Zinks, welche sich auf ihr ablagern, geht
diese erhöhte Thätigkeit bald verloren. Da nämlich dieser Niederschlag den
Wasserstoff stark anzieht, so wird dieser auf der Platte zurückgehalten, welche dann
von Gas umhüllt und dadurch von der Flüssigkeit der Batterie abgesondert ist. Die
gewöhnlichen Lösungsmittel der Metalle entfernen diese Decke von Unreinigkeit nicht
leicht. Die Platte kann durch neues Platiniren wieder hergestellt werden; da dieses
aber lästig und kostspielig ist, so bemühte ich mich ein Auflösungsmittel zu finden,
welches geeignet wäre, dem Platin seine frühere Wirkung wieder zu ertheilen, und
erreichte diesen Zweck durch Eintauchen der Platte in eine Lösung von
Eisenchlorid.
Nun wurden die Platten täglich in das Eisenchlorid getaucht, und so die Spannung der
Batterie constant erhalten. Durch diese Entdeckung, verbunden mit der Verwendung
besserer Auflösungen für die Zersetzungszelle, wurde die Zeit zur Herstellung einer
galvanischen Platte abgekürzt; sie war aber, wenn nur ein einziges Element benutzt
wurde, noch zu lang.
Die effective Kraft einer Batterie kann durch eine zweite verstärkt werden; auf diese
Weise wird E in der Formel vergrößert und dadurch unter
Umständen auch eine Vergrößerung von Q
hervorgerufen.
Wir vereinigen die Wirkung mehrerer Batterien, indem wir die ungleichen Pole der
Reihe nach verbinden. Da bei einer solchen Anordnung der Strom jede Batterie in der
Kette durchziehen muß, so vervielfacht sich R ebenso wie
E, und die Formel wird dann Q
=
nE/(nR + r). Sind die Werthe von R
und r nahezu gleich (wozu die Batterien besonders
construirt werden können), so wird es eine Frage von Wichtigkeit, ob man durch
Verbindung der gleichnamigen Enden aller Zellen den Apparat als einziges Element,
oder ob man durch Verbindung der ungleichnamigen Pole eine Batterie von zwei Paaren
herstellen soll. Durch Bildung zweier Elemente wird R
verdoppelt, zugleich wird aber die Oberfläche halb so groß und die Kette noch einmal
so lang, wodurch sich R vervierfacht und statt Q = E/(R + r) hat man Q = 2 E/(4 R + r). Ist R = r, so wird Q = 0,50 bei der Herstellung nur eines Elementes, und
Q = 0,40 bei der Herstellung zweier; man erhält also
bei der doppelten Auslage eine langsamere Ablagerung als vorher. Ist R = 10 r, so erhält man mit
einer einfachen Batterie Q = 1/(1 + 10) = 0,0909; für
zwei solche in einer Reihe aufgestellte Batterien wird Q
= 2/(2 + 10) = 0,166. Die Anwendung von zwei Batterien, aufeinanderfolgend
aufgestellt, verdoppelt also die Auslagen, aber nicht den Effect, und die Rücksicht
auf Ersparung verbietet uns eine fernere Vergrößerung der Reihe. Für einen doppelten
Effect von E/(R + r) hat man
Textabbildung Bd. 138, S. 355
Da die Division von R durch 2
einer Verdoppelung der Batteriefläche gleich kommt, so wird nun Q = 0,182 und der Gewinn in Procenten zeigt an, daß es
bei Verdoppelung der Oberfläche vortheilhaft ist, die Vergrößerung dann eintreten zu
lassen, wenn zwei Batterien (Glieder) hinter einander angewendet werden.
Die Schwierigkeit große ebene Silberplatten zu erhalten, war ein bedeutendes
Hinderniß der Vergrößerung der Batterieoberfläche, weil man wegen der
Unregelmäßigkeit der Oberfläche der Silberplatte dieselbe weiter von dem Zink
entfernen muß, wodurch R vergrößert und dem eigentlichen
Zweck entgegengewirkt wird. Man könnte die Silberplatten mit dem Abschlichthammer
ebnen, aber diese Arbeit ist mit Kosten verbunden, und da die Platten beim Gebrauch
beständig Unfällen ausgesetzt sind, so wäre diese Methode nicht ökonomisch. Obwohl
die Versilberung der Metalle im Großen mit Erfolg betrieben wird, ist es doch nicht
gelungen, leicht und billig galvanoplastische Silberplatten herzustellen, und alle Versuche Platten von
2500 Gran Gewicht per Quadratfuß zu erhalten, schlugen
fehl. Durch Aenderung der Silberlösungen und Anwendung einer Registerbatterie (register battery) gelang es uns aber in 30 Stunden eine
vollkommen ebene Platte herzustellen, welche in hohem Grade die erforderliche Härte,
Elasticität und Hämmerbarkeit besaß, während die Herstellungskosten per Unze nicht über 16 Cents betrugen. Die vollkommen
ebenen Platten gestatten eine sehr bedeutende Annäherung an das Zink. Man kann sie
daher über doppelt so groß als früher anwenden, weil bei der Anordnung von zwei
Gliedern hinter einander r verhältnißmäßig kleiner
bezüglich R ist.
Man hatte längst beobachtet, daß Temperaturwechsel auf die Dauer des Processes von
Einfluß sind, und jeder, der sich mit Elektrometallurgie beschäftigt, weiß wie
wichtig es ist, das Laboratorium warm zu halten. Um zu ermitteln, wo und wie die
Wärme wirkt, wurde bei 60º F. (15º,56 C.) eine Batterie mit einem 120
Fuß langen Draht verbunden und ein Galvanometer eingeschaltet. Die Ablenkung betrug
40º. Nun kühlte man die Batterie auf 48º F. (8º,89 C.) ab, und
die Nadel zeigte noch immer nahezu 40º.
Dieser Versuch beweist, daß die Batterien durch den gewöhnlichen Temperaturwechsel
nicht bedeutend afficirt werden, und dieser Umstand wurde nun benutzt, um eine
vollkommenere Ventilation herzustellen. Es wurde nämlich durch eine Glaswand ein
kleiner Platz für die Batterie von dem allgemeinen Local getrennt und am Boden und
der Decke mit großen Oeffnungen nach außen versehen, um eine Circulation der Luft
herzustellen und dadurch die Dämpfe der Batterie wegzuführen.
Mittelst Anwendung aller beschriebenen Verbesserungen
konnte man nun leicht in 8–10 Tagen eine galvanoplastische Platte von 8
Quadratfuß herstellen. Von dem Wunsche durchdrungen, den Proceß noch mehr zu
beschleunigen und wo möglich ein Pfund Kupfer täglich auf den Quadratfuß
niederzuschlagen, suchte ich noch weitere Verbesserungen zu machen. Da E der Formel bereits so groß war, als die Kosten es
gestatteten, und R soviel als möglich verkleinert, d. i.
die Platten möglichst vergrößert waren, so suchte ich dem Q durch Verminderung von r, dem
elektrolytischen Widerstande, einen höheren Werth zu geben. Dem Elektrolyten durch
Zusatz leicht zersetzbarer Salze ein besseres Leitungsvermögen zu ertheilen, wurde
ohne Erfolg versucht. Da sich nun, wie bereits erwähnt, ergeben hat, daß die
beschleunigende Wirkung der Wärme sich hauptsächlich auf die Zersetzungszelle
beschränkt, so war offenbar durch Anwendung der höheren Temperatur bei dem Elektrolyten
ausschließlich, ein großer Vortheil zu erwarten.
Um die vortheilhafteste Temperatur und den durch sie zu erzielenden Gewinn an Wirkung
zu bestimmen, wurde eine mit Voltameter versehene Batterie mit zwei Elektroden in
Verbindung gebracht, die in eine Lösung tauchten, wie sie bereits als allgemein
empfohlen erwähnt worden ist. Jede Elektrode war 5 Quadratzoll groß und hinten
gefirnißt um die Ausstrahlung zu verhüten. Nun brachte man sie in eine gegenseitige
Entfernung von einem Zoll, und dünne Holzplatten an ihren Rändern verhüteten jeden
seitlichen Verlust des zwischen ihnen durchgehenden Stromes. Die Resultate waren
folgende:
Die Batterieplatten
in
Berührung
gaben
stündlich
300
Kubikzoll
Gas
Die Elektroden
„
„
„
„
216
„
„
Als der
Strom bei
58º F.
durch
den Elektrolyt ging,
gab
er stündlich
16
Kubikzoll
Gas
„
„
60º
„
„ „
„
„
20
„
„
„
„
100º
„
„ „
„
„
27
„
„
„
„
175º
„
„ „
„
„
37
„
„
Um den Werth des Widerstandes der Lösung, im Vergleich mit R der Formel, zu bestimmen, verband man zuerst die Batterieplatten, und
hernach die Elektroden; er beträgt
für
58º
F
23,15
60º
18,15
100º
13,00
175º
8,96
Aus vorstehender Tabelle erhellt, daß der Widerstand in der Zersetzungszelle von 2,58
auf 1, im Ganzen von 2,25 auf 1 vermindert wurde. Da nun
Textabbildung Bd. 138, S. 357
so kann man durch Erwärmung des Elektrolyten eine Platte bei
Verwendung eines einzigen Elementes eben so schnell machen, als bei gewöhnlicher
Temperatur mit einer Batterie von zwei Elementen und je der doppelten Oberfläche
(4mal die Batterie, 2mal die Auslage).
Smee's Vorschriften verlangen, daß zur Anfertigung einer
Platte gewisse gegenseitige Verhältnisse des verwendeten Apparates aufrecht erhalten
werden; daraus folgt, daß wenn die Temperatur des Elektrolyten auf einen gewissen
Grad erhöht, und der Apparat ihr entsprechend eingerichtet worden ist, man, um nicht
unaufhörlich corrigiren zu müssen, die anfängliche Wärme unterhalten muß. Will man
nun die durch die Temperaturerhöhung gebotenen Vortheile benützen, so ist ein
weiterer Apparat unbedingt nöthig, der die hohe Temperatur in dem Elektrolyten während mehrerer
Tage zu unterhalten vermag. Da die elektrotypischen Operationen bei Nacht nicht
unterbrochen werden, so muß der Heizapparat wenigstens 12 Stunden ohne Aufsicht und
ohne Nachschüren seinen Dienst leisten und die ganze Zeit hindurch constant wirken.
Ich habe einen solchen Ofen erfunden, den man nun benutzt. Ein Peck (7 1/5 Liter)
Holzkohlen genügt, um ihn 12 Stunden lang zu heizen und er erhält 100 Gallons (363
Liter) Kupferlösung auf jeder verlangten Temperatur zwischen 100 und 200º F.
(38 und 93º C.).
Mittelst der beschriebenen Anordnung habe ich eine große Copie (als Relief)
dargestellt und das mir übergebene Original nach 55 Stunden wieder abgeliefert.
Um zu der Ohm'schen Formel zurückzukehren, wurde das
Verhältniß von R zu r von
Neuem durch einen Versuch bestimmt. Das Resultat war R :
r = 1 : 4 oder Q = 1/(1
+ 4) = 0,20, ein großer Fortschritt, wenn man die erste Bestimmung R : r = 1 : 19 oder Q = 1/(1
+ 19) = 0,05 damit vergleicht. Da nun r im Vergleiche
mit R so klein geworden ist, so kann man die
Batterieoberfluche so lange mit Nutzen vergrößern, bis das Resultat etwa 0,24 ist.
Wenn man überdieß die Elemente zu je zweien mit doppelten Oberflächen anwendet, um
den doppelten Effect zu bekommen, so ergibt sich 2 . 1/(1 + 4) = 2/(2 + 4) = 0,40.
Da nun der relative Widerstand im Elektrolyten noch kleiner wird, so kann man die
Batterieoberfläche noch mehr vergrößern, bis das Resultat nahezu 0,5 ist.
Ich habe in der letzten Zeit (1851) Platten von vorzüglicher Qualität, drei Pfund
Kupfer per Quadratfuß enthaltend, in 24 Stunden
dargestellt, wornach für unsere größten Platten von 10 Quadratfuß Oberfläche und 1/8
Zoll Dicke nur zwei Tage erforderlich wären.
Vorgänge in der elektrolytischen Lösung. – Die
Güte des abgelagerten Metalles hängt einzig und allein von dem Verhältnisse ab,
welches zwischen der durch eine Lösung ziehenden Elektricitätsmenge und dem
Metallgehalt dieser Lösung besteht.
Man nimmt gewöhnlich an, daß die Säure des Salzes an die eine, das Metall an die
andere Elektrode gehe; es ist aber jetzt erwiesen, daß dem nicht so ist, denn
während die Säure sich an die positive Elektrode begibt, gelangt das Metall nicht an die negative Elektrode. Daher kommt es, daß wenn
die Lösung beim Beginn des Processes noch so concentrirt war, die negative Elektrode doch
bald mit einer schwachen Lösung umgeben ist, weil diese Elektrode der Lösung in
ihrer Nähe das Metall entzogen hat. Besteht die Elektrode bloß aus einem Draht, so
wird die sie umgebende erschöpfte Lösung leicht wieder erneuert, da durch die bloße
Verschiedenheit des spec. Gewichtes eine Strömung entsteht. Bei großen Elektroden,
bestehend in Platten die einander parallel sind, wird aber die schnelle Erneuerung
der concentrirten Lösung unmöglich, und die Elektrode ist bald mit einer schwachen
Lösung umgeben. Auf diesen Umstand muß bei der Herstellung der Batterien Rücksicht
genommen werden. Wer ihn nicht kennt, findet zu seinem Erstaunen, daß ihm große
Platten mißglücken, während Medaillen und kleinere Platten vollkommen gelingen.
Auf den ersten Blick sollte man glauben, daß durch Anwendung einer stärkern
Kupfervitriollösung ein rascheres Nachschaffen des Metalles zur Elektrode erzielt
würde. Leider wird aber dadurch das Lösungsvermögen des in der Flüssigkeit
enthaltenen Wassers für das an der positiven Elektrode durch die Wirkung der
übertragenen Säure gebildete Sulphat vermindert. Dünnflüssigkeit ist das
Wesentlichste bei der Elektrolyse; wenn z.B. die Menge des freien Wassers welches
die positive Elektrode umgibt, klein ist, so ist diese Elektrode bald in eine
gesättigte Lösung gehüllt, und das neugebildete Salz bleibt ungelöst auf ihr liegen;
da dieses Salz nicht leitet, so schließt es die Elektrode von der Flüssigkeit ab und
hält so den Strom auf, bis der Abfluß der gesättigten Lösung es dem Salze ermöglicht
sich aufzulösen, worauf dem Strome der Durchgang wieder geöffnet wird. Bei solcher
unterbrochenen Wirkung erhält man Platten von Kupfersand, oder bisweilen Kupfer
welches so weich wie Blei ist.
Erwärmt man die Flüssigkeit wenn ein solcher Zustand eingetreten ist, so wird das
Lösungsvermögen des Wassers für das Salz erhöht, es entsteht eine rasche Diffusion,
das Salz wird zur negativen Elektrode geführt und das erschöpfte Wasser zur
positiven Elektrode; die eingeschlafene Batterie kommt in ununterbrochene
Thätigkeit, und in kurzer Zeit hat sich eine Platte abgelagert, welche alle Härte
und Elasticität des gehämmerten oder gewalzten Kupfers besitzt.
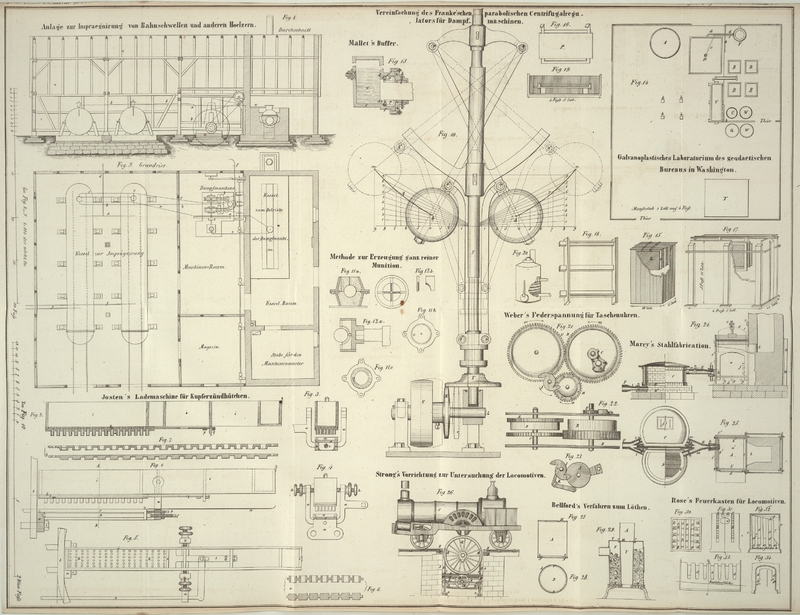
Apparate des galvanoplastischen Laboratoriums. –
Fig. 14
ist der Grundriß des Laboratoriums des geodätischen Bureaus in Washington.
Die Glaswand b, b, b, b ist mit einer Thür versehen und
trennt das Batteriezimmer von dem allgemeinen Laboratorium; sie gestattet also die
Batterie leicht zu beaufsichtigen, ohne daß man deren Dämpfen ausgesetzt ist. Der
Fußboden des Laboratoriums ist etwa 6 Fuß über dem Erdgeschoß und neigt sich einwärts von den
Seiten gegen die Abzugslöcher h, h, h, h, welche die auf
den Boden gegossenen unbrauchbaren Flüssigkeiten und das Spülwasser abführen. Um den
schädlichen Wirkungen zu entgehen, denen man beim Arbeiten ausgesetzt ist, wenn der
Boden von chemischen Agentien durchdrungen ist, wird derselbe, nachdem Flüssigkeiten
weggeschüttet wurden, gehörig überschwemmt und abgebürstet.
An den Stellen B, B, B, B sind vier Batteriezellen
angebracht. Ein länglich-viereckiger Behälter von Kautschuk, welcher in einem
tiefen hölzernen Kasten steht, enthält die Batterie-Auflösungen. Jede Zelle
kann 9 Silber- und 8 Zinkplatten aufnehmen. Eine Metallleitung verbindet alle
Zinkplatten, und eine andere alle Silberplatten einer Zelle. Jede Zelle kann als
unabhängige Batterie benutzt werden, oder man kann 2,3
oder 4 Zellen mit einander in beliebiger Ordnung verbinden. Die verticale
Zersetzungswanne ist bei V, die horizontale bei H. S ist eine große Kufe zum Abwaschen der Platten. Die
Kufe C enthält die Eisenchloridlösung. Q ist der Quecksilberkasten, und W, W sind Kufen mit frischem Wasser. F ist der
Ofen, und d, d, c, c sind Heizröhren die mit der Wanne
H in Verbindung stehen. T ist ein flacher eiserner Tisch.
Fig. 15 zeigt
eine Zelle mit ihren Platten, nebst deren Aufhängungsweise.
Fig. 16 ist
der Holzrahmen, mit seiner Platte P, welche zum
Eintauchen in die verticale Wanne hergerichtet ist.
Fig. 17 ist
die verticale Wanne mit den in ihr hängenden Platten.
Fig. 18 zeigt
den adjustirbaren, die Platte haltenden Holzrahmen, welcher in der horizontalen
Wanne gebraucht wird.
Fig. 19 zeigt
die Anordnung im Innern der horizontalen Wanne; eine bildlose Platte und ein
gravirtes Original sind in der erforderlichen Lage angebracht; die mit ihnen
verbundenen Kupferdrähte gehen zu der Batterie.
Fig. 20 zeigt
den Heizofen. Die Thür für den Luftzutritt befindet sich bei a und ist mit einem adjustirenden, aus Eisen und Zink zusammengesetzten
Stabe so verbunden, daß man sie mittelst einer Stellschraube zum Reguliren des Zuges
anordnen kann, indem der Stab dann die Thür öffnet und schließt, wodurch eine
gleichförmige Wärme in der Lösung unterhalten wird. Nachdem das Feuer angezündet
ist, muß die Thür sich schließen, wenn die Auflösung eine Temperatur von 180º
F. (82º C.) erreicht hat. Im Ofen ist ein bleiernes Schlangenrohr angebracht,
dessen Enden c und d (Fig. 14) zu
der horizontalen Wanne führen; das Ende c verbindet den
obern Theil der Wanne gerade unter der Oberfläche der Flüssigkeit mit dem obern
Theile des Schlangenrohres, und d den Boden der Wanne mit
dem untern Theile des Schlangenrohres. Es entsteht daher eine Circulation der Lösung
vom Ofen aus nach dem Obertheil der Wanne und von deren Boden aus nach dem Ofen.
Verfahrungsweise. – Soll eine Platte elektrotypirt
werden, so bringt man sie auf Gestelle über die offenen Abzugslöcher h, h, h, h, und wascht sie sorgfältig mit Alkalien und
Säuren. Hierauf wird sie versilbert, jodirt und vor ein Fenster gestellt
(belichtet). Nun wählt man eine Platte von gewalztem Kupfer, welche einen Zoll
größer ist, als die gravirte Platte, legt sie auf den ebenen eisernen Tisch und
klopft sie so lange mit einem hölzernen Schlägel, bis ein Stahllineal zeigt, daß sie
eben ist; sie wird dann gewogen und mit zwei kupfernen Haken in dem verticalen
Plattenrahmen befestigt. In gleicher Weise wird die gravirte Platte in einem
ähnlichen Rahmen befestigt, worauf beide in eine verticale Wanne gestellt und mit
der Batterie verbunden werden.
Der Proceß geht zwar nicht gut von statten, wenn die Platten vertical stehen, aber
man muß ihnen im Anfange diese Stellung geben, um zu verhüten, daß sich Staub und
Flecken von Unreinigkeiten auf ihrer Oberfläche absetzen. So wie sich die gewalzte
Platte auflöst, machen ihre Verunreinigungen die Auflösung schnell trübe, und
gefährden die Oberfläche der sich bildenden Platte. Gewöhnlichen Elektrotypen
schaden Staub und Schmutzflecken nicht, da aber die Kupferplatten des geodätischen
Bureaus in Feinheit der Linien feinen Stahlplatten nicht nachstehen, so bewirken die
auf der Bildfläche ihrer Copien sich absetzenden Unreinigkeiten daß deren Abdrücke
ein wolkiges Ansehen erhalten. Bei dem ersten Eintauchen der Platten sollte daher
die Lösung vollkommen rein seyn.
Früher wurde die verticale Wanne nach jedem Gebrauch geleert und ausgewaschen.
Nachdem die Lösung ihren Niederschlag abgesetzt hatte, wurde sie abgezogen und durch
sehr feine Baumwolle geseiht. Dieses Verfahren war sehr lästig und beschäftigte
einen Arbeiter einen ganzen Tag. Durch ein einfaches Auskunftsmittel bewerkstelligte
ich, daß man die Wanne nur noch einmal monatlich zu reinigen braucht. Um die neue
Platte vor Staub und Schmutz zu schützen, wird ein Sack von feiner Baumwolle über
einen leichten Holzrahmen gezogen, der ihn ausgespannt erhält; eine Stunde bevor man
die Lösung braucht, wird der Sack mit dem darin eingeschlossenen Rahmen auf die
Lösung gelegt und mit den Kupferstäben beschwert, welche sonst die Plattenrahmen
halten. Das Gewicht veranlaßt den Sack allmählich zu sinken, und während des
Hinabsinkens filtrirt er die in der Wanne enthaltene Lösung; die Unreinigkeiten können die Maschen des
Gewebes nicht ganz verstopfen, weil dasselbe während des Sinkens stets mit neuen
Portionen von Flüssigkeit in Berührung kommt. So wird nun die Flüssigkeit mit
Vermeidung von Arbeit und Zeitverlust filtrirt, ohne daß man sie aus dem Gefäß nimmt
oder den Bodensatz aufstört.
Die Platte bleibt über Nacht in der verticalen Wanne und am Morgen werden die
Vorbereitungen getroffen, um sie in die horizontale Wanne zu versetzen. Zuerst wird
der Ofen in Thätigkeit gesetzt. Eine neue bildlose Kupferplatte, einen Zoll größer
als die Matrize, wird auf dem eisernen Tisch eben geplättet, und an den Kanten von
Holzstäben mit Bolzen von Platin befestigt, damit sie auf diese Weise horizontal
gehalten, nicht niedersinken kann. Nun nimmt man die überzogene Matrize aus der
verticalen Wanne, befreit sie von ihrem Rahmen und bringt sie in den horizontalen
Rahmen. Eine hölzerne Einfassung von der Höhe eines Zolles umgibt dann die Platte,
und auf diese Einfassung wird die erwähnte bildlose Platte gelegt, worauf man das
Ganze in die horizontale Wanne bringt und die Verbindung mit der Batterie herstellt.
Dann nimmt man die positive Platte aus der verticalen Wanne, und bestimmt und notirt
sich ihren Gewichtsverlust. Mittelst des bekannten Flächeninhalts der Matrize
berechnet man die Menge Kupfer, welche zu einem Abgusse (Copie) von 1/8 Zoll Dicke
erforderlich ist. Der Betrag des in beiden Wannen verzehrten (bildlosen) Kupfers muß
diesem Quantum gleich kommen, bevor die erforderliche Dicke erreicht ist (nach einem
Abzug für die Verunreinigungen des gewalzten Kupfers und für die Rauhigkeit der
Hinterseite des Elektrotypes). Nach wenigen Stunden hat sich die eingelegte bildlose
Platte so mit Unreinigkeiten beladen, daß diese auf das Elektrotyp zu fallen
beginnen, daher diese Platte aus der Wanne entfernt und sogleich durch eine neue
ersetzt werden muß. Die schmutzige Platte wird dann in dem großen Wassertroge
gewaschen und nach der Reinigung ihr Gewichtsverlust bestimmt und notirt. Aus dem
erlittenen Gewichtsverlust kann man auf die Wirkung der Batterien schließen. Jetzt
muß man die Batterien und das Verhältniß der Kupferablagerung in einer bestimmten
Zeit sorgfältig überwachen, und die Batteriestärke nach den Umständen abändern.
Die ganze thätige Batterie braucht in der Regel nur einmal täglich erneuert zu
werden, wobei man auf folgende Weise verfährt: Man nimmt eine Zinkplatte und eine
Silberplatte aus der Batterie; die Silberplatte steckt man in die
Eisenchloridlösung, die Zinkplatte aber bringt man zu der Wasserkufe vor der Thür
des Batterielocals und scheuert sie mit einer steifen Bürste rein, worauf man sie an
dem Quecksilberkasten wieder amalgamirt und dann in die Batterie zurückbringt. Die Silberplatte
kommt jetzt aus der Eisenchloridlösung in die nahe stehende Kufe mit frischem
Wasser. Nun bringt man eine zweite Silberplatte aus der Batterie in die
Chloridlösung, dann wird eine andere Zinkplatte gereinigt, gewaschen und mit der
ersten Silberplatte in die Batterie zurück gebracht. Auf diese Weise kann man die
ganze Batterie erneuern, ohne ihre Wirkung wesentlich zu unterbrechen.
Wenn der Gewichtsverlust des gewalzten Kupfers in beiden Wannen anzeigt, daß das
Elektrotyp die erforderliche Dicke erlangt hat, so wird die Platte von der Batterie
weggenommen, von ihrem Rahmen befreit, ihre Hinterseite glattgehobelt und ihre
Ränder abgefeilt, bis die Trennung stattfinden kann. Nach der Trennung ist das
Original frei; das erhaltene Relief wird genau so wie ein Original versilbert und
elektrotypirt, und die Copie desselben ist bei guter Ausführung der Operationen ein
vollkommenes Facsimilie des Originals, an Härte, Dehnbarkeit und Elasticität den
besten gewalzten und gehämmerten Kupferplatten nicht nachstehend.
Tafeln