| Titel: | Elektro-chemisches Verfahren, um Blei und Braunstein aus Auflösungen abzuscheiden, in welchen sie enthalten sind. Von Hrn. Becquerel, vorgelesen an der Académie des Sciences, am 3. Mai 1830. |
| Fundstelle: | Band 38, Jahrgang 1830, Nr. LV., S. 178 |
| Download: | XML |
LV.
Elektro-chemisches Verfahren, um Blei und
Braunstein aus Aufloͤsungen abzuscheiden, in welchen sie enthalten sind. Von Hrn.
Becquerel,
vorgelesen an der Académie des Sciences, am 3. Mai
1830.
Aus den Annales de Chimie et de Physique. 13. Bd. S.
380.
Mit Abbildung auf Tab.
V.
Becquerel, elektro-chemisches Verfahren um Blei und
Braunstein aus Aufloͤsungen abzuscheiden.
Sobald man die Entdekung gemacht hatte, daß die galvanische Saͤule die
Eigenschaft besizt Saͤuren und salzige Aufloͤsungen mittelst zweier
Platinnaplatten zu zersezen, die in dieselben eingetaucht sind, und wovon jede mit
einem der beiden Enden des Apparates in Verbindung steht, fand man auch, daß
Sauerstoff und Saͤuren immer gegen den positiven Pol hingefuͤhrt
werden, und Wasserstoff und Basen gegen den negativen Pol. In dem Falle, wo die
Aufloͤsung mehrere Verbindungen enthaͤlt, hat also auf jeder Seite
eine Mischung von Koͤrpern von derselben Natur Statt, welche der chemischen
Analyse zur Abscheidung uͤberlassen bleibt. Wenn man diese Abscheidung
mittelst der galvanischen Saͤule bewerkstelligen will, so muͤssen die
Apparate so vorgerichtet werden, daß die Natur einiger Elemente dadurch
geaͤndert wird, ohne daß die uͤbrigen, mit welchen sie verbunden oder
gemengt sind, dadurch litten.
Die zahlreichen Untersuchungen, welche ich uͤber die bestehenden
Verhaͤltnisse zwischen den Verwandtschaften und den elektrischen
Kraͤften angestellt habe, sezten mich auch in den Stand diese Frage in
Hinsicht auf das Blei und den Braunstein zu loͤsen, und es ist mir
wahrscheinlich, daß man auch bei anderen Metallen aͤhnliche Resultate
erhalten wird, wenn man ihre elektro-chemischen Eigenschaften gehoͤrig
studiert.
Die Elektricitaͤt kann also, wie man sehen wird, als sehr empfindliches
Reagens nicht bloß zur Entdekung des in den Aufloͤsungen enthaltenen Bleies
und des darin befindlichen Braunsteines dienen, sondern selbst noch dieselben mit
Leichtigkeit daraus abscheiden, so daß keine Spur mehr von denselben darin
zuruͤkbleibt, und ohne daß man zu besorgen haͤtte, daß andere Metalle
zugleich mit den selben daraus entfernt wuͤrden. Es scheint mir, daß diese
Resultate fuͤr die Chemie nuͤzlich seyn koͤnnen. Ehe ich die
Grundsaͤze entwikle, auf welchen die elektro-chemische Analysirmethode
beruht, von welcher ich so eben gesprochen habe, will ich den Apparat und das
Verfahren beschreiben, dessen ich mich bediene.
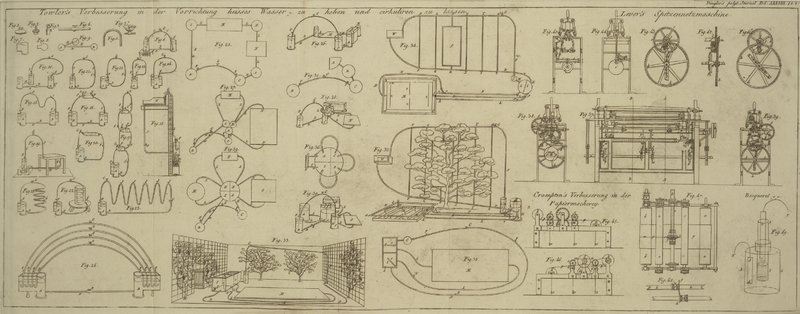
Man nimmt ein Trinkglas, AA, Fig. 49., und gießt
salpetersaure Kupferaufloͤsung in dasselbe. Hierauf taucht man eine
Roͤhre bb
' in dieselbe, deren unterer Theil mit Thon
gefuͤllt ist, welcher mit einer Aufloͤsung von essigsaurer Soda etwas
befeuchtet wurde, und gießt in den oberen Theil derselben eine Aufloͤsung von
essigsaurem Eisen. Eine Platinnaplatte, cc
', welche mit dem positiven Pole einer galvanischen
Saͤule von geringer Spannung (welche z. B. nur aus
Einem Plattenpaare besteht) verbunden ist, taucht in die essigsaure
Eisenaufloͤsung, und eine andere Kupferplatte, dd
', welche mit dem negativen Pole in Verbindung steht,
taucht in die salpetersaure Kupferaufloͤsung. In dem Augenblike, wo der
Apparat anfaͤngt zu wirken, wird das Kupfer, indem das salpetersaure Kupfer
sich unter dem Einflusse sehr schwacher elektrischer Kraͤfte leicht zersezt,
sich auf der Platte des gleichnamigen Metalles reduciren, waͤhrend der
Sauerstoff und die Salpetersaͤure in die andere Roͤhre
uͤbergehen werden, wo der Sauerstoff sich zum Theile entwikelt,
waͤhrend die Salpetersaͤure das essigsaure Eisen zersezt, da sie sich
mit dem Eisen verbindet und die Essigsaͤure verjagt. Da die Wirkung dieser
Saͤule zu schwach ist, um fuͤr sich selbst die essigsaure Verbindung
zu zersezen und die Uebertragung des Eisenoxydes nach dem negativen Pol zu
bestimmen, so ist die nothwendige Folge diese, daß alle gebildeten Producte in der
Roͤhre bleiben. Die Platinnaplatte behaͤlt ihren Glanz; welchen sie
vor dem Versuche hatte. Wenn man der Aufloͤsung des essigsauren Eisens nur
einen einzigen Tropfen essigsauren Braunstein zusezt, der nur ein Tausendstel Gramm
von diesem Salze enthaͤlt, und selbst noch weniger, so wird die
Platinnaplatte, welche der positive Pol ist, auf der Stelle eine leichte Bisterfarbe
annehmen. Wenn man die Menge des essigsauren Braunsteines vermehrt, so wird die
Farbe noch dunkler, und am Ende ganz schwarz. Diese Gegenwirkung hat so lang Statt,
als Braunstein im essigsauren Eisen vorhanden ist; das, was also die Platinnaplatte
auf obige Weise faͤrbt, ist das Braunsteinperoxyd. Bei diesem Versuche hat nun
Folgendes Statt. Die Platinnaplatte aͤußert gegen die Aufloͤsungen der
essigsauren Verbindungen eine zersezende Kraft, ohne jedoch die Zersezung derselben,
wegen der geringen Spannung der Saͤule vollkommen bewirken zu koͤnnen;
der Sauerstoff aber und die Salpetersaͤure, die in die Aufloͤsung
gelangen, vollenden die Zersezung, indem der Sauerstoff den Braunstein, und
wahrscheinlich auch das Eisen, uͤberoxydirt, und die Salpetersaͤure
die Essigsaͤure verjagt, die frei wird. Da nun das Braunsteinperoxyd in der
Essigsaͤure unaufloͤsbar ist, so sezt es sich auf der Platinnaplatte
als ein Haͤutchen ab, dessen Theilchen ein metallisches Ansehen besizen,
waͤhrend das Eisenperoxyd, wenn sich eines bildet, in den Saͤuren
aufgeloͤst bleibt.
Ich bediente mich einer Saͤule mit geringer Spannung, um dasjenige, was
waͤhrend des Versuches Statt hat, desto deutlicher kennen zu lernen. Eine
gewoͤhnliche Saͤule gibt aber dasselbe Resultat. Man gießt in eine
Porzellankapsel die essigsaure Eisen- und Braunsteinaufloͤsung, und
taucht dann zwei Platinnaplatten in dieselbe, deren jede mit einem Pole der
Saͤule in Verbindung steht. Es wird alsogleich Zersezung des Wassers und
Gasentwikelung Statt haben. Der Sauerstoff, der sich nach dem positiven Pole begibt,
uͤberoxydirt den Braunstein, welcher dann die Essigsaͤure
verlaͤßt, und sich, wie vorher, auf der positiven Platinnaplatte absezt. Man
sieht nun, warum das salpetersaure Kupfer nothwendig war, wenn man die galvanische
Saͤule nur unter geringer Spannung anwendete: da das Wasser nicht zersezt
war, so mußte man sich Sauerstoff und eine staͤrkere Saͤure, als
Essigsaͤure, verschaffen. Die leichte Zersezung des salpetersauren Kupfers
gewaͤhrte den einen und die andere. Schwefelsaurer und salpetersaurer
Braunstein fuͤhren zu demselben Resultate, wie der essigsaure, indem das
Braunsteinoxyd in Schwefel- und Salpetersaͤure unaufloͤsbar
ist. Die angefuͤhrten Versuche wurden hier aber vorzuͤglich mit
essigsaurem Braunstein angestellt.
Man kann sich kein einfacheres Verfahren denken, als diese Weise, den Braunstein von
dem Eisen abzuscheiden. Es ist bloß noͤthig, eine Aufloͤsung dieser
Metalle in Essigsaͤure zu bilden, und hinlaͤnglich große
Platinnaplatten, und eine hinlaͤnglich starke galvanische Saͤule zu
nehmen, wenn der Versuch rasch von Statten gehen soll. Wenn man mit kleinen
Quantitaͤten zu thun hat, so reichen zuweilen einige Stunden hin, zumal, wenn
man die Vorsicht braucht, von Zeit zu Zeit das Peroxyd, das sich auf der positiven
Platinnaplatte absezt, wegzunehmen. Wenn die Aufloͤsung ein Gramm essigsauren
Braunstein enthaͤlt, sind 24 Stunden nothwendig, zuweilen noch mehr: ich
wiederhole jedoch, daß die Zeit von der Groͤße der Platten und von der Spannung der
Saͤule abhaͤngt. Wenn die Platte aufhoͤrt sich zu
faͤrben, kann man sicher seyn, daß die Aufloͤsung keinen Braunstein
mehr enthaͤlt oder hoͤchstens nur eine unbestimmbar geringe Menge
desselben, indem man auf diese Weise den tausendsten Theil eines Grammes, und selbst
noch weniger, wenn er in Wasser aufgeloͤst ist, bestimmen kann.
In dem Verhaͤltnisse, als die Zersezung Statt hat, wird die
Fluͤssigkeit immer mehr und mehr sauer; aus diesem Grunde sezt sich nur wenig
Eisenoxyd auf die negative Platte ab, weil es alsogleich wieder zum Theile
aufgeloͤst wird. Wenn die Operation vollendet ist, waͤscht man diese
Platte mit der Saͤure, um das wenige Eisenoxyd aufzuloͤsen, welches
sich auf derselben findet, und das Braunsteinperoxyd zu sammeln, das sich daselbst
anhaͤngen konnte.
Es moͤgen was immer fuͤr Metalle mit dem Braunstein verbunden seyn, man
wird lezteren auf diese Weise immer leicht davon abscheiden. Ich will hier nur des
Zinkes und des Braunsteines erwaͤhnen, die, nach dem gewoͤhnlichen
chemischen Verfahren, so schwer von einander zu scheiden sind.
Gegen Ende der Arbeit wird die Fluͤssigkeit oͤfters rosenfarben, und,
nach einiger Zeit darauf, wieder farbenlos, wenn die Wirkung der galvanischen
Saͤule aufgehoͤrt hat. Dieß ruͤhrt davon her, daß die
Saͤule auf das Tritoxyd reducirend wirkt, folglich eine geringe Menge dieses
Salzes auf ein Minimum der Oxydation herabzusezen strebt. Wenn die Operation aber
fortgesezt wird, so hoͤrt sie mit Zersezung dieses lezteren auf, so daß
nichts mehr in der Aufloͤsung uͤbrig bleibt. Ich habe mich bei diesen
Versuchen eines Trogapparates (pile à auge) von
30 Paar Scheiben bedient, von 8 Centimeter Hoͤhe und 6 Centimeter Breite. Sie
waren, um ihre Wirkung zu verlaͤngern, mit einer leichten
Kochsalzaufloͤsung belegt. Staͤrkere Saͤulen koͤnnten
vielleicht, indem sie die Essigsaͤure zersezen, Wirkungen erzeugen, die den
beabsichtigten entgegen waͤren, insofern man Braunsteinperoxyd erhalten will.
Die Abscheidung des Bleies von anderen Metallen fordert einige Abaͤnderungen
an dem hier oben angegebenen Verfahren, welches darin besteht, daß man eine Kapsel
mit einer Aufloͤsung der essigsauren Verbindungen fuͤllt, und zwei
Platinnaplatten in dieselben taucht, wovon jede mit einem Pole einer
gewoͤhnlichen galvanischen Saͤule in Verbindung steht: bei dem Bleie
kann diese Vorrichtung nicht angewendet werden, indem das Oxyd sich leicht reduciren
laͤßt; das Metall wirft sich alsogleich auf die negative Platinnaplatte, so
wie die uͤbrigen in der Aufloͤsung enthaltenen Grundlagen. Mit
Saͤulen von geringer Spannung, und mit dem Apparate in Fig. 1. ist man diesem
Nachtheile nicht ausgesezt. Das Blei verhaͤlt sich hier wie der Braunstein, d.h., es
uͤberoxydirt sich, und sezt sich auf der positiven Platinnaplatte ab. Das
Haͤutchen des Peroxydes ist oͤfters schwarz und krystallinisch; wenn
man es zerreibt, kommt die Flohfarbe (puce) wieder zum
Vorscheine. Da aber Saͤulen mit schwacher Spannung nur langsam wirken, so muß
man, wo mit einer gewoͤhnlichen Saͤule gearbeitet wird, dieselbe so
vorrichten, daß das Bleioxyd nicht auf den negativen Pol gefuͤhrt werden
kann, wo eine Reduction Statt haben wuͤrde. Man erreicht diesen Zwek, wenn
man sich desselben Apparates bedient, den man bei der gewoͤhnlichen
voltaïschen Saͤule spielen laͤßt. Auf diese Weise macht man
nicht bloß die kleinsten Bleitheilchen bemerkbar, die sich in der Aufloͤsung
befinden, sondern man schafft sie zugleich auch alle so vollkommen heraus, daß
selbst die empfindlichsten chemischen Reagentien, wie schwefelwasserstoffsaures
Ammonium, nicht mehr im Stande sind Spuren davon zu entdeken, wenn die Operation ein
Mal vollendet ist. Die Mittel, Bleiperoxyd von Braunsteinperoxyd zu unterscheiden,
sind aus der Chemie bekannt, und beduͤrfen hier keiner Erwaͤhnung.
Essigsaures Silber, aus Kapellensilber, reducirt das Blei sehr schnell, so wie auch
das salpetersaure Silber. Man kann also dieses Verfahren mit Erfolg anwenden, um
Blei aus allen Aufloͤsungen zu beseitigen, in welchen es sich befindet. Der
Vortheil, den man hierbei, so wie bei dem Braunsteine hat, ist, daß man sich
Operationen erspart, die oft mehr oder minder bedeutenden Verlust bei der Analyse
veranlassen.
Aus dem Obenerwaͤhnten erhellt nun der Vortheil, den man von der Wirkung der
galvanischen Saͤule bei der chemischen Analyse erhalten koͤnnte, wenn
man die elektro-chemischen Eigenschaften aller einfachen Koͤrper
genauer kennte. Es ist wahrscheinlich, daß man dahin gelangen wuͤrde, sie wie
Blei und Braunstein von einander zu scheiden. Neue Resultate werden uns vielleicht
in den Stand sezen, diesen Untersuchungen noch eine weitere Ausdehnung zu geben, die
der Chemie nuͤzlich werden kann.
Tafeln